Cập Nhật Chẩn Đoán Và Điều Trị Vô Sinh Không Tắc Nghẽn (Non-Obstructive Azoospermia – NOA)
Trung tâm Sức khoẻ Nam Giới Men's Health
Vô sinh không tắc nghẽn (NOA) là một trong những nguyên nhân nghiêm trọng nhất gây vô sinh nam, xảy ra khi tinh hoàn không thể sản xuất tinh trùng dù đường dẫn tinh vẫn thông suốt. Đây không chỉ là vấn đề y khoa phức tạp, mà còn ảnh hưởng sâu sắc đến tâm lý và hạnh phúc gia đình. Việc chẩn đoán và điều trị NOA đòi hỏi sự kết hợp giữa kiến thức sinh lý sinh sản, công nghệ hỗ trợ sinh sản và tư vấn tâm lý cho bệnh nhân.

1. Tổng quan về vô sinh không tắc nghẽn
NOA chiếm khoảng 60% trường hợp vô tinh (azoospermia) ở nam giới. Khác với vô sinh do tắc nghẽn (Obstructive Azoospermia – OA), tình trạng này liên quan trực tiếp đến rối loạn quá trình sinh tinh (spermatogenesis). Các nguyên nhân thường gặp gồm bất thường di truyền (như hội chứng Klinefelter, mất đoạn AZF trên nhiễm sắc thể Y), rối loạn nội tiết (hypogonadotropic hypogonadism), hoặc tổn thương tinh hoàn do viêm, chấn thương, xạ trị, hóa trị.
Theo nghiên cứu của Jarow và cộng sự (2021) công bố trên The Journal of Urology, tỷ lệ NOA ở nam giới vô sinh dao động 1% trong dân số nói chung nhưng chiếm tới 10–15% trong nhóm bệnh nhân nam đến khám vì hiếm muộn, với độ tuổi trung bình 32,5 ± 5,8 năm.
2. Cơ chế bệnh sinh
Quá trình sinh tinh diễn ra trong ống sinh tinh (seminiferous tubules) của tinh hoàn, được điều hòa bởi hormone FSH (Follicle-Stimulating Hormone) và testosterone. Ở NOA, sự rối loạn này có thể xuất phát từ:
- Suy sinh tinh nguyên phát (primary testicular failure): tế bào mầm không phát triển hoặc thoái hóa sớm, dẫn đến ống sinh tinh xơ hóa.
- Rối loạn điều hòa nội tiết: thiếu hụt GnRH (Gonadotropin-Releasing Hormone) hoặc tổn thương tuyến yên làm giảm FSH/LH.
- Tổn thương do yếu tố ngoại lai: hóa trị, xạ trị, nhiễm virus quai bị sau dậy thì.
Cơ chế này được xác nhận qua mô bệnh học. Theo nghiên cứu của Esteves et al. (2015) trên Human Reproduction Update, phân tích sinh thiết tinh hoàn ở bệnh nhân NOA cho thấy 55% có hội chứng chỉ tế bào Sertoli (Sertoli cell-only syndrome), 25% ngừng trưởng thành tinh trùng ở giai đoạn sớm (maturation arrest) và 20% xơ hóa hoàn toàn ống sinh tinh.
3. Chẩn đoán
Chẩn đoán NOA cần sự phối hợp của nhiều bước, nhằm phân biệt với OA và xác định nguyên nhân.
- Khai thác tiền sử và khám lâm sàng
Bác sĩ sẽ tìm hiểu tiền sử dậy thì, chấn thương, bệnh lý tinh hoàn, tiếp xúc hóa chất, tiền sử gia đình. Khám lâm sàng đánh giá thể tích tinh hoàn (bình thường 15–20 mL), mức độ lông mu, hình thái dương vật, dấu hiệu bất thường di truyền.
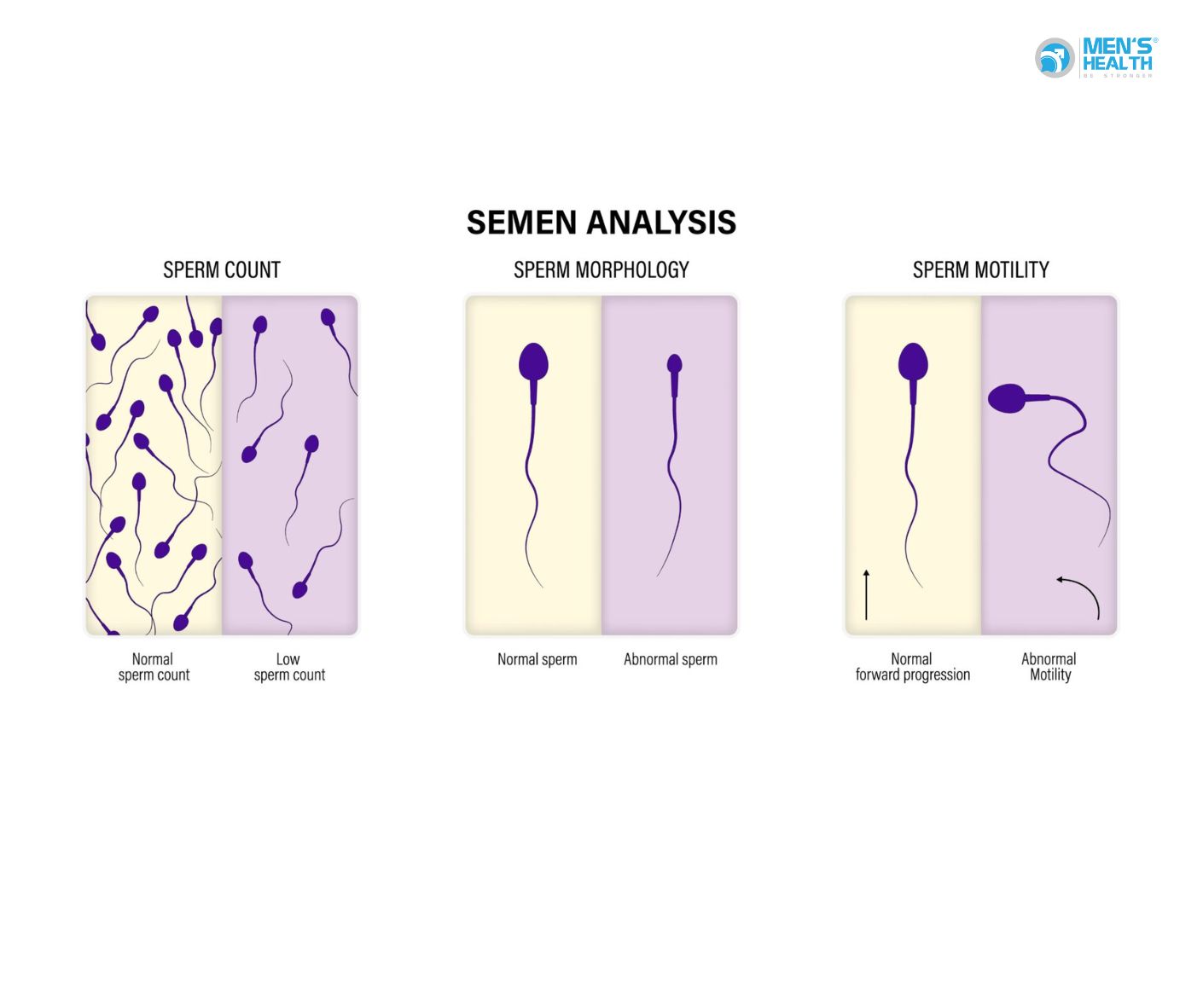
- Xét nghiệm tinh dịch đồ (Semen analysis)
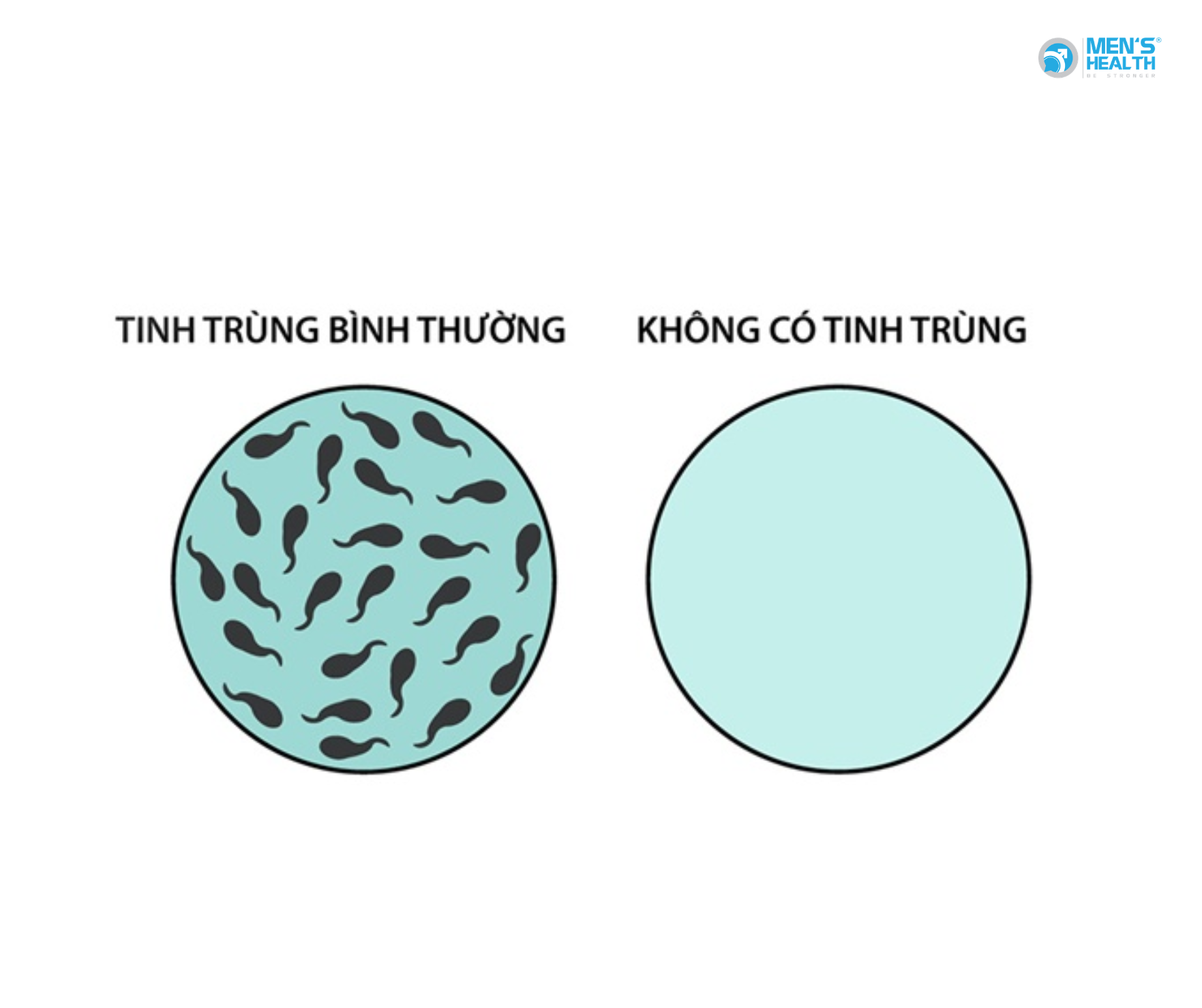
Ít nhất 2 lần xét nghiệm, cách nhau 2–4 tuần, sau kiêng xuất tinh 2–7 ngày. Ở NOA, không tìm thấy tinh trùng dù ly tâm mẫu.
- Xét nghiệm nội tiết
Định lượng FSH, LH, testosterone toàn phần (total testosterone), estradiol, prolactin. NOA thường kèm FSH tăng (>12 IU/L) và testosterone bình thường hoặc giảm.
d. Xét nghiệm di truyền
- Nhiễm sắc thể đồ (karyotype) để phát hiện hội chứng Klinefelter (47,XXY).
- PCR tìm mất đoạn AZFa, AZFb, AZFc trên nhiễm sắc thể Y.
- Hình ảnh học và sinh thiết tinh hoàn (Testicular biopsy)
Siêu âm bìu giúp loại trừ OA do tắc nghẽn. Sinh thiết xác định mô học, đồng thời phục vụ thu tinh trùng nếu có.
4. Điều trị
Điều trị NOA tập trung vào 2 mục tiêu:
(1) Tối ưu hóa điều kiện nội tiết và sức khỏe toàn thân để cải thiện khả năng sinh tinh.
(2) Thu nhận tinh trùng bằng các kỹ thuật vi phẫu để sử dụng trong thụ tinh trong ống nghiệm (IVF/ICSI).
Liệu pháp nội tiết
Áp dụng khi có rối loạn trục dưới đồi–tuyến yên–tinh hoàn (hypogonadotropic hypogonadism). Tiêm hCG kết hợp FSH tái tổ hợp có thể phục hồi sinh tinh sau 6–12 tháng.
Phẫu thuật vi phẫu tìm tinh trùng (micro-TESE)
Đây là tiêu chuẩn vàng cho NOA. Dưới kính hiển vi phẫu thuật, bác sĩ chọn các ống sinh tinh giãn to – nơi có khả năng chứa tinh trùng cao nhất. Tỷ lệ thành công dao động 40–60% tùy nguyên nhân. Theo nghiên cứu của Bernie et al. (2015) trên Fertility and Sterility, micro-TESE cho tỷ lệ tìm được tinh trùng cao hơn đáng kể so với TESE truyền thống (57% so với 33%, p<0,01).
Bảo tồn và trữ lạnh tinh trùng
Nếu tìm được tinh trùng, cần trữ lạnh ngay để sử dụng cho ICSI, tránh nguy cơ thất bại ở lần mổ sau.

Hỗ trợ tâm lý
NOA gây áp lực tinh thần lớn. Tư vấn giúp bệnh nhân và bạn đời hiểu rõ tình trạng, giảm cảm giác tội lỗi hoặc mất tự tin.
5. Trường hợp lâm sàng
Trường hợp 1
Nam bệnh nhân 34 tuổi, đã kết hôn 3 năm nhưng chưa có con. Khám lâm sàng: tinh hoàn nhỏ (10 mL hai bên), lông mu thưa. Tinh dịch đồ 2 lần: không có tinh trùng. Xét nghiệm nội tiết: FSH 21,3 IU/L, LH 8,7 IU/L, testosterone 11,2 nmol/L. Karyotype 46,XY, mất đoạn AZFc.
Bệnh nhân được tư vấn micro-TESE. Ca mổ thu được ít tinh trùng, trữ lạnh và dùng cho ICSI. Sau 2 chu kỳ IVF, vợ bệnh nhân có thai và sinh con khỏe mạnh.
Khuyến cáo của TS.BS.CK2 Trà Anh Duy: Với mất đoạn AZFc, cơ hội tìm tinh trùng vẫn có, nhưng cần tiến hành sớm vì chức năng sinh tinh có thể suy giảm nhanh.
Trường hợp 2
Nam bệnh nhân 29 tuổi, tiền sử hóa trị lymphoma 5 năm trước. Thể tích tinh hoàn 12 mL, lông mu bình thường. Tinh dịch đồ: không có tinh trùng. FSH 18,5 IU/L, testosterone 14,1 nmol/L. Sinh thiết tinh hoàn cho thấy xơ hóa lan tỏa, không tìm thấy tinh trùng. Bệnh nhân được tư vấn sử dụng tinh trùng hiến.
Khuyến cáo của TS.BS.CK2 Trà Anh Duy: Nên trữ lạnh tinh trùng trước hóa trị/xạ trị để tránh mất hoàn toàn khả năng sinh tinh.
6. Tiến bộ và xu hướng tương lai
Công nghệ sinh học đang mở ra hy vọng mới cho bệnh nhân NOA:
- Nuôi cấy tinh nguyên bào (spermatogonial stem cell culture): nghiên cứu trên động vật cho thấy khả năng tạo tinh trùng ngoài cơ thể.
- Chỉnh sửa gen CRISPR-Cas9: tiềm năng sửa chữa đột biến gây vô sinh di truyền.
- Liệu pháp tế bào gốc (stem cell therapy): thử nghiệm giai đoạn đầu cho kết quả khả quan, nhưng cần nghiên cứu dài hạn.
Theo nghiên cứu của Yoshida et al. (2023) công bố trên Nature Communications, cấy ghép tế bào gốc dòng mầm đã phục hồi một phần quá trình sinh tinh ở mô hình chuột NOA, tỷ lệ xuất hiện tinh trùng di động đạt 23,5%.
7. Kết luận
NOA là thách thức lớn trong điều trị vô sinh nam. Chẩn đoán chính xác, kết hợp điều trị nội tiết hợp lý và vi phẫu micro-TESE, đã giúp nhiều bệnh nhân có cơ hội làm cha. Tuy nhiên, hiệu quả còn phụ thuộc nguyên nhân và thời điểm can thiệp. Trong tương lai, các tiến bộ về tế bào gốc và chỉnh sửa gen có thể thay đổi hoàn toàn tiên lượng bệnh, nhưng hiện tại, tư vấn kịp thời và lựa chọn chiến lược cá nhân hóa vẫn là chìa khóa.
 0902 353 353
0902 353 353 Giờ làm việc: 08:00 - 20:00
Giờ làm việc: 08:00 - 20:00 7B/31 Thành Thái, Phường Diên Hồng, TP. HCM
7B/31 Thành Thái, Phường Diên Hồng, TP. HCM